2.2. Первичные химические источники тока
К первичным ХИТ относятся источники тока, активные вещества которых используются однократно. Рассмотрим особенности конструкции таких элементов, механизмы токообразующих процессов и эксплуатационные характеристики ХИТ данного типа.
Сухие марганцово-цинковые (МЦ) элементы
Первичные сухие ХИТ выпускаются промышленностью с не проливающимся электролитом (загущенным крахмалом, мукой, карбоксиметилцеллюлозой (КМЦ)). Типичным представителем сухих ХИТ являются МЦ-элементы стаканчиковой и галетной конструкций, в которых используют солевые (NH4Cl) и щелочные (NaOH, KOH) электролиты [4–6]. Схематически их можно представить так:
Активными веществами анода и катода являются цинк Zn и диоксид марганца MnO2 соответственно. Концентрация щелочного электролита составляет 6–10 М, что отвечает максимуму электропроводности и минимальной температуре замерзания раствора.
Устройство щелочного марганцово-цинкового элемента показано на рис. 2. Цинковый анод располагается в цилиндрической камере внутри элемента и представляет собой пасту на основе порошка цинка. Пространство между сепаратором и корпусом заполняется смесью диоксида марганца с угольным порошком – это активная катодная масса. В качестве положительного коллектора тока служит стальной корпус элемента. Сепаратор, а также анодная и катодная активные массы пропитаны электролитом для снижения внутреннего сопротивления элемента.
Рис. 2. Схема щелочного марганцово-цинкового элемента
Диоксид марганца восстанавливается на катоде. В щелочных растворах реакция протекает с участием молекул воды:
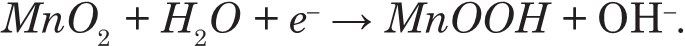
Потенциал электрода зависит от активностей MnО2 и MnOOH [4].
На поверхности зерна положительной активной массы, в которую для повышения ее электропроводности добавляют графит (рис. 3), образуется фаза переменного состава хMnOOH(1–x)MnO2.
Рис. 3. Активная масса положительного электрода МЦ-элемента
После насыщения ею поверхностного слоя активной массы система становится неравновесной, идет диффузия протонов вглубь зерна, постепенно восстанавливаются глубинные слои активной массы [5, 6].
Из-за замедленности диффузии в твердой фазе концентрация манганита в поверхностном слое и в объеме активной массы выравнивается только после включения нагрузки.
Анодное растворение цинкового электрода в щелочных растворах имеет свои особенности. Первичный процесс
связан с расходом относительно большого количества щелочи – двух ионов ОН– на каждый прошедший электрон. В реакции образуется цинкат K2[Zn(OH)4], растворимость которого в щелочных растворах менее 1–2 М. После насыщения раствора цинкатом на поверхности цинка начинается осаждение гидроксида цинка:
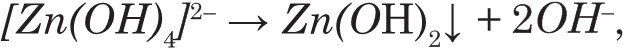
и первичный процесс прекращается. Следовательно, емкость цинкового электрода определяется количеством щелочи.
При малой плотности тока электрод работает и в насыщенном цинкатном растворе. Вторичный процесс идет с образованием нерастворимых соединений цинка:
Расход ионов ОН– во вторичном процессе сокращается вдвое по сравнению с первичным и практически в процессе щелочь вообще не расходуется. Для работы элемента необходим небольшой объем электролита, который затрачивается на заполнение межэлектродного пространства и пор электродов.
В современных щелочных марганцово-цинковых элементах преимущественно используется вторичный процесс окисления цинка. Применяются порошковые пастообразные цинковые электроды. За счет большой площади их истинной поверхности резко снижается плотность тока, что является предпосылкой для протекания вторичного процесса. Раствор электролита предварительно насыщают цинкатом за счет растворения в нем оксида цинка.
Суммарные токообразующие реакции в щелочном марганцово-цинковом элементе могут быть представлены следующими уравнениями:
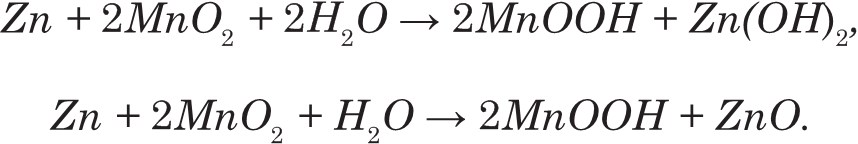
Напряжение разомкнутой цепи щелочного марганцово-цинкового элемента находится в диапазоне 1,5–1,7 В. Как и у всех химических источников тока, емкость элементов с щелочным электролитом уменьшается при увеличении тока разряда.
При непрерывном разряде средними и повышенными токами щелочные элементы обеспечивают емкость до 7–10 раз большую, чем солевые элементы тех же габаритов. Щелочные элементы лучше работают в области низких температур: при –20 °С они обладают такой же емкостью, что и солевые в режиме непрерывного разряда при комнатной температуре.
Скорость побочного коррозионного окисления цинка в растворе щелочного электролита невелика. Выделение водорода на цинке по уравнению
протекает медленно, так как электролит насыщен продуктом коррозии – цинкатом. Для дополнительного снижения скорости коррозии цинк может быть легирован свинцом, индием, висмутом и алюминием, в отдельных случаях вводят ингибиторы коррозии. В итоге скорость саморазряда щелочных марганцово-цинковых элементов очень мала: после 1 года хранения при 20 °С потери емкости не превышают 10 % от начального значения. Гарантийный срок хранения щелочных элементов достигает 10 лет.
Щелочные марганцово-цинковые элементы применяются для электропитания устройств с высоким токопотреблением – фотовспышка, мощный электрический источник света, или требующих длительного непрерывного разряда – цифровые фотоаппараты, плейеры, диктофоны.
Первичные ХИТ с литиевыми анодами
Первичные ХИТ с литиевыми анодами считаются в настоящее время наиболее перспективными, что обусловливается уникальными свойствами лития.
Литий имеет высокий электроотрицательный потенциал и обладает наименьшим теоретическим расходом металла на единицу емкости. Литий имеет низкое удельное сопротивление и высокую химическую активность. Он корродирует в газах, энергично реагирует с водой:
Поверхность лития покрывается слоем оксида или гидроксида и пассивируется. Чистый металл может реагировать с большинством органических и неорганических веществ. Это ограничивает выбор активных масс, электролитов, конструкции литиевых элементов и условия их производства.
Для работы с литием используют атмосферу сухого инертного газа, а содержание воды в апротонных растворителях и солях лития жестко контролируется. В ХИТ с литиевыми анодами применяют и расплавы чистых солей или их эвтектических смесей.
Катодной активной массой в литиевых ХИТ служат оксиды металлов (V2O5, MnO2,WO3, CuO, TiO2, MoO3) и некоторых неметаллов (SOCl2, SO2), а также фториды углерода, халькогениды, сульфиды железа, меди или титана. В большинстве случаев процессы восстановления активной массы происходят в твердой фазе. Литий ведет себя как электрод первого рода.
Механизм восстановления оксидов в апротонных безводных растворителях отличается от процессов восстановления в водной среде тем, что роль катиона водорода играет катион лития, который внедряется в кристаллическую решетку оксида:
Внедрение катиона лития в нестехиометрические оксиды происходит без нарушения строения кристаллической решетки [4]. Для оксидов с малым объемом элементарной ячейки кристалла внедрение Li+ сопровождается ее разрушением.
На процессы электровосстановления катодных материалов оказывает влияние природа растворителя.
Элементы на основе апротонных растворителей, в которых используется диоксид марганца, широко применяются в радиоэлектронной и вычислительной аппаратуре. Они имеют большую удельную энергию, малый саморазряд, хорошо сохраняются и работают в достаточно широком диапазоне температур.
Наряду с неводными органическими, в литиевых гальванических элементах используются и неорганические растворители. Литий-тионилхлоридный элемент отличается тем, что SOCl2 служит как в качестве окислителя, так и растворителя для тетрахлоралюмината лития LiAlCl4. Катодная и токообразующая реакции описываются уравнениями:
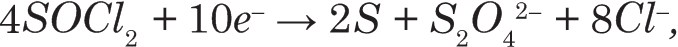
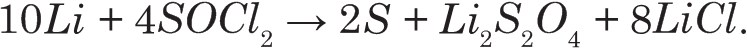
Электрохимическая система элемента:
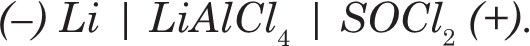
При номинальном стабильном напряжении 3,4 В и хороших эксплуатационных характеристиках – мощности, сроке годности и низкотемпературных характеристиках, такой элемент обеспечивает потребности в электропитании многих военных и космических аппаратов. Однако его применение в бытовой технике сильно ограничено из-за токсичности тионилхлорида, а также высокой пожаро- и взрывоопасности элемента.
Твердотельный литий-йодный элемент используется для питания имплантируемых электрокардиостимуляторов. Обеспечивая малый ток, он является компактным, безопасным и надежным. Электрохимическая система элемента может быть записана в следующем виде:
Токообразующая реакция в элементе является полностью твердофазной:
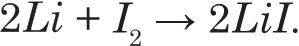
Катод – смолистый материал, который образуется при реакции полимера поли-2-винилпиридина с избытком йода, с формулой (mI2?[CH2CH(C5H5N)]n). Соединение обладает заметной электронной проводимостью. Литий-йодный элемент содержит слой этого вещества на литиевой фольге.
Твердый электролит – иодид лития формируется в ходе разряда элемента на стыке между электродами и постепенно увеличивается в толщину в ходе разряда. Образующийся слой имеет достаточную проводимость, чтобы обеспечить гарантированную работу устройства в течение не менее 8 лет.
Эффективность характеристик первичных ХИТ с литиевыми анодами снижается в зависимости от катодных материалов в ряду:
ХИТ с твердым электролитом
Твердые электролиты, применяемые в ХИТ, не должны иметь смешанную ионно-электронную проводимость, которая способствует возникновению коротких замыканий в элементе.
Достаточно высокую ионную проводимость при комнатной температуре имеют двойные соли на основе хорошо проводящих ток иодидов серебра RbAg4I5 [4]. В качестве катодных активных веществ и анодов используют полииодиды и серебро соответственно. Известно применение электролитов на основе диоксидов циркония или ?-алюминатов натрия.
На основе твердых электролитов, являющихся одновременно и сепараторами, сконструированы низкотемпературные миниатюрные элементы и батареи разной конструкции. Они обладают большой механической прочностью, очень малым саморазрядом и большим сроком службы. В пленочных конструкциях твердый электролит наносят на пластиковую сетку, прижимаемую электродами. Толщина батареи ХИТ, используемой для кардиостимуляторов, при площади электродов 1 см2 составляет всего 100 мкм.
Разряд большинства элементов с твердыми электролитами ведут малыми токами, а последовательно соединенные элементы с небольшим разрядным напряжением могут давать высокое напряжение. Подобные ХИТ используют в лабораторной технике для подзаряда конденсаторов, питания приборов с высокими омическими сопротивлениями, в электронных часах, для устройств защиты памяти в ЭВМ. Примеры некоторых электрохимических систем с твердыми электролитами и их характеристики приводятся ниже:
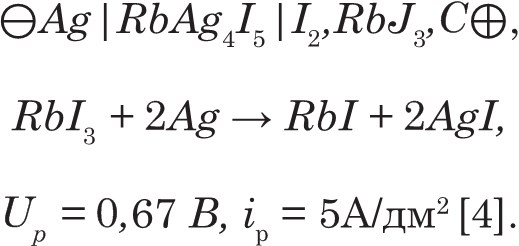
К преимуществам ХИТ с твердыми электролитами следует отнести высокие удельные энергии; пологие разрядные характеристики в широком интервале рабочих температур; практически неограниченный срок годности; миниатюрность и герметичность конструкций, безопасность эксплуатации. Применяют элементы в устройствах с малым потреблением энергии и длительным сроком службы.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.