Плюс химия
Плюс химия
Теперь мне стало ясно, почему на автомобили устанавливают обычные электроаккумуляторы, а не конденсаторы или сверхпроводящие магниты.
Действительно, автомобильные аккумуляторы могут месяцами хранить энергию, причем в достаточно большом количестве. Я сам видел, как иногда автомобили «гоняют на стартере»: включают стартер, питаемый от аккумуляторов, вроде бы для заводки двигателя, но привода на колеса при этом не отключают, как положено по инструкции, – и машина катит по улице. А ведь энергия аккумулятора здесь расходуется не только на движение автомобиля, но и на прокрутку двигателя. Не будь этой прокрутки, автомобиль смог бы пройти «на стартере» больше километра – настолько велика емкость аккумуляторов. Похоже, известные всем нам автомобильные электроаккумуляторы пока ближе всего к «энергетической капсуле».
Позвольте, но так ли уж они известны? Однажды ко мне пришел знакомый мальчик лет шести и в разговоре сказал, что знает, как устроен телевизор. На мой вопрос, может ли он нарисовать его схему, мальчик ответил утвердительно. Однако удивление мое быстро прошло, когда вместо схемы он изобразил переднюю панель телевизора. «Это экран, это ручка громкости, это яркость…» – перечислял он.
Вот так же и я представлял себе электроаккумулятор – пластмассовый ящик с клеммами, внутри которого находятся пластины и кислота, часто называемая «аккумуляторной». Что происходит внутри аккумулятора, каким образом он накапливает энергию – все это было мне невдомек.
Оказалось, что я не одинок в своем неведении. Никто из водителей, которых я расспрашивал о принципе работы аккумулятора, не дал вразумительного ответа. Мне говорили: он накапливает энергию потому, что к клеммам подсоединяется генератор или выпрямитель, которые и подают в аккумулятор ток. После этого уже сам аккумулятор становится источником тока до тех пор, пока не разрядится. Вроде бы понятно. А почему таким свойством обладает именно аккумулятор, а не кирпич, например? Да потому, дескать, что он так устроен.
Этих сведений мне было явно недостаточно. Пришлось в который раз сесть за книги.
История электроаккумуляторов берет начало со знаменитого опыта, проделанного итальянским физиком Алессандро Вольтой в 1799 году. Ученый опустил медный и цинковый электроды в разбавленную серную кислоту и обнаружил, что между электродами возникла разность потенциалов. Соединив электроды проводником – проволочкой, Вольта получил электрический ток. Тем самым он доказал, что различные металлы, помещенные в растворы кислот, образуют источник тока.
Это был первый в мире гальванический элемент, названный так в честь итальянского физика и врача Луиджи Гальвани, который еще до Вольты заметил появление тока при взаимодействии двух разных металлов, замыкаемых через живую ткань – лапку препарированной лягушки. Гальвани, правда, считал, что это электричество «животное» и вырабатывается оно мышцами.
Правда, есть сведения, что гальванические элементы существовали и в древности. Во время археологических раскопок были найдены глиняные кувшины с напоминающими электроды цилиндрами из разных металлов, причем некоторые ученые считают, что электролитом тогда служили вино или уксус. И будто бы с помощью этих элементов древние мастера умели делать гальванические покрытия: например, наносили тончайшую пленку золота или серебра на украшения.
Древняя электрическая батарейка
Так или иначе, огромная заслуга Вольты состоит в том, что он не только построил гальванический элемент, но и объяснил его действие, чего по вполне понятным причинам не могли сделать древние.
Элемент Вольты давал очень маленькое напряжение. Чтобы повысить его, стали изготавливать батареи из медных и цинковых пластин, переложенных прокладками, смоченными серной кислотой. Батареи эти, названные вольтовыми столбами, обеспечивали уже достаточно большое напряжение. После Вольты немало ученых – Жорж Лекланше, Якоб Даниэль, Вильям Грове и
Угольный электрод

Вольтов столб
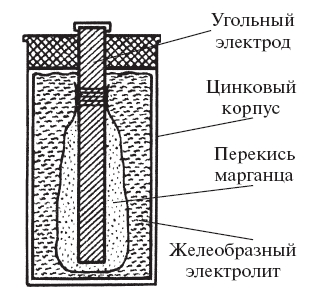
«Сухая» батарейка на основе элемента Лекланше
Лекланше, твердые – цинковый стаканчик и графитовый стержень. А вот электролит уже не жидкий. Ведь жидкость может в любой момент пролиться, а делать элемент герметичным дорого и сложно. Вот и заменили жидкость желеобразным электролитом. Получился удобный и практичный источник электричества.
Если через разряженную сухую батарею особыми импульсами пропустить ток, ее можно вновь «оживить». Эту операцию порой проделывают по несколько раз. Однако она ненадолго восстанавливает элемент.
Постойте-постойте… Как бы там ни было, получается, что гальванический элемент – тот же аккумулятор! Заряжая его электрическим током, восстанавливая, мы накапливаем в нем электроэнергию, которую затем расходуем. Так ли это?
Оказывается, и так и не так. Прежде всего, не каждый гальванический элемент можно подзарядить. Нельзя это сделать, например с элементом, который состоит из двух электролитов. Таков элемент Даниэля, где две разные жидкости разделены пористым стаканчиком. Постепенно просачиваясь через стаканчик, электролиты смешиваются, реагируют друг с другом и выделяют ток. Этот элемент, если он уже отработал свой срок, не восстановишь.
Другие элементы с твердыми электродами в принципе подзаряжаются, накапливают энергию. Но процесс накопления столь неэкономичен и неэффективен, что многие считают подзарядку таких элементов неоправданной. Накапливается только ничтожная часть поданной на элемент электроэнергии, а сам элемент после нескольких таких зарядок разрушается. Чтобы стать хорошим накопителем, гальванический элемент должен достаточно хорошо «переносить» процесс зарядки. И этого наконец удалось добиться в середине XIX века.
В 1859 году французский ученый и инженер Гастон Планте провел любопытный опыт, внешне очень похожий на опыт Вольты. Как и Вольта, Планте построил гальванический элемент, однако в качестве электродов он взял две свинцовые пластины, в обычных условиях покрытые пленкой окиси свинца. Электролит был все тот же – разбавленная серная кислота. Планте подключил к электродам источник постоянного тока и некоторое время пропускал ток через свой элемент, совсем как при подзарядке сухих элементов. Потом он отключил ток и подключил к электродам гальванометр. Прибор показал, что гальванический элемент сам стал вырабатывать электроток и при этом выделять почти всю энергию, затраченную на его зарядку. Зарядку можно было повторять много раз: элемент неизменно работал исправно и не разрушался, подобно сухим батареям.
Этот гальванический элемент назвали элементом второго рода, или аккумулятором.
Как же происходит накопление энергии в аккумуляторе Планте? При пропускании тока через электролит из серной кислоты на свинцовой пластине, соединенной с отрицательным полюсом источника тока – катодом, – выделяется водород, который восстанавливает окись свинца в чистый свинец. На электроде, соединенном с положительным полюсом – анодом, – выделяется кислород, который окисляет окись свинца до перекиси. Аккумулятор зарядится в тот момент, когда катод целиком станет чистым свинцом, а анод – перекисью свинца. Тогда между электродами окажется наибольшее напряжение.
Соединяя пластины-электроды проводником с потребителем, расходуя энергию, мы разряжаем аккумулятор. Направление тока при разрядке противоположно тому, что было при зарядке. Положительно заряженная пластина будет восстанавливаться водородом, а отрицательная – окисляться кислородом. Как только пластины станут одинаковыми, аккумулятор прекратит давать ток. Надо повторить зарядку.
Ясно, что энергия в таком аккумуляторе накапливается не в виде электрического или магнитного поля, как в предыдущих накопителях электрической энергии, а в виде вполне осязаемого вещества – свинца, переходящего с выделением энергии в перекись свинца. Сам процесс накопления и выделения энергии здесь происходит иначе, нежели в чисто электрических аккумуляторах – конденсаторах и электромагнитах. Поэтому такой аккумулятор принято называть электрохимическим.
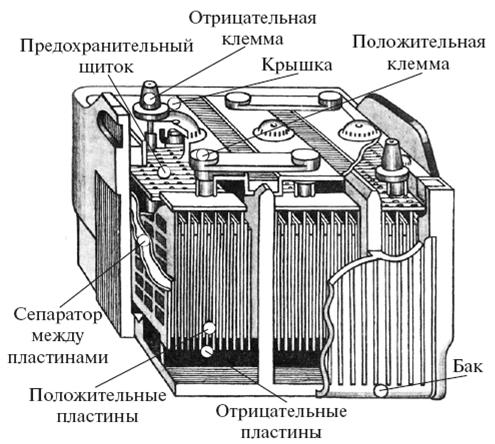
Свинцово-кислотный аккумулятор
В конструкциях автомобильных свинцово-кислотных аккумуляторов ученые постарались как можно больше увеличить поверхность электродов, не нарушая при этом их прочности. Ведь именно от величины поверхности зависит энергоемкость аккумулятора. Сейчас пластины аккумулятора изготовляют в форме свинцовых решеток, покрытых перекисью свинца (положительный электрод) и губчатым свинцом (отрицательный электрод). Электролитом служит 25—35%-ный водный раствор серной кислоты. Заряженный автомобильный аккумулятор имеет напряжение (точнее, электродвижущую силу) на клеммах 2-2,2 В. При разрядке это напряжение падает, и когда оно достигает 1,8 В, разрядку обычно прекращают, иначе решетка из свинца может слишком истончиться в ходе реакции, и пластины, потеряв прочность, рассыплются.
Мне очень хотелось узнать, что будет с аккумулятором, если попробовать хотя бы кратковременно получить от него ток большой мощности. Однажды я упросил одного знакомого водителя включить стартер, питаемый, как известно, от аккумулятора, при не включенном двигателе. Двигатель, естественно, не завелся, а секунд через 15—20 стартер начал сбавлять обороты. Еще через некоторое время он вообще остановился. Было полное впечатление, что аккумулятор разрядился и больше из него «выжать» ничего нельзя. Я думал, водитель рассердится, скажет, мол, видишь, к чему привели твои опыты. Но он неторопливо выключил стартер, а потом, спустя пару минут, снова включил его. Стартер заработал! Откуда взялись «силы» у аккумулятора? Не мог же он, как живое существо, «отдохнуть»!
В самом деле, поведение аккумулятора и живого организма здесь поразительно похожи. При усталости мышц от интенсивной работы их сила резко снижается, и нужно время, чтобы силы восстановились. Человек сделает гораздо больше, если он будет работать без спешки, неторопливо, с постоянной, но умеренной нагрузкой. Например, если попытаться бегом подняться на 20-й этаж дома, – без остановок это вряд ли получится, потребуется отдых. Да и с остановками усталость будет ощущаться немалая. А если идти спокойно, то 20 этажей можно преодолеть без особых усилий.
Так и в аккумуляторе: при включении его на большую мощность серная кислота, которая находится в порах пластин, быстро израсходуется, в результате реакции она превратится в воду, и выделение тока прекратится. Только через некоторое время, когда серная кислота постепенно вновь заполнит поры, можно опять разряжать аккумулятор.
Поэтому разряжают и заряжают аккумуляторы – это касается практически всех видов электрохимических аккумуляторов – обычно с достаточно малой нагрузкой, небольшими токами и продолжительное время – несколько часов. Здесь и кроется один из главнейших недостатков электрохимических аккумуляторов – их малая мощность, приходящаяся на килограмм массы аккумулятора, так называемая удельная мощность, или иначе – плотность мощности.
Свинцово-кислотные аккумуляторы весьма экономичны, однако они и капризны, часто портятся, недолговечны. К тому же свинец – сравнительно редкий и дорогой металл, а кислота – опасна в обращении. Естественно, что ученые стали искать новые материалы и новые принципы работы аккумуляторов. Так возник второй основной тип электрохимических аккумуляторов – щелочные аккумуляторы. Создание их тесно связано с именем знаменитого американского ученого и изобретателя Томаса Эдисона. Знаменитый изобретатель «всех времен и народов» Томас Алва Эдисон был моим кумиром. Я очень хотел походить на него стремлением к цели и работоспособностью, правда, не всегда удачно мне это удавалось.
В аккумуляторах Эдисона электролитом служит уже не кислота, а щелочь – 20%-ный раствор едкого кали. Пластины изготовлены из стальных решеток с карманами. У положительных пластин карманы заполнены смесью, содержащей окись никеля, а у отрицательных – губчатым кадмием. Корпус щелочного аккумулятора стальной, что придает устройству большую прочность.
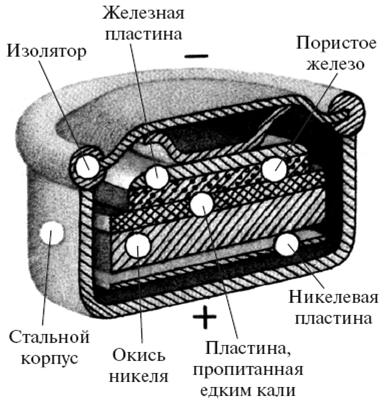
Щелочной «кнопочный» аккумулятор
Щелочные аккумуляторы дороже кислотных и менее экономичны. Но, несмотря на это, в них больше достоинств, чем недостатков – они неприхотливы, прочны, долговечны. Поэтому они находят все большее применение в технике. Например, на троллейбусах применяются именно такие накопители. Их можно видеть также в транзисторных приемниках, телефонных и слуховых аппаратах, карманных фонариках и в других устройствах. Во многих радиоприборах присутствуют миниатюрные аккумуляторы, тоже щелочные, под названием «кнопочные», так как они внешне напоминают кнопку. Ценность их состоит в том, что они герметично закрыты, совершенно нечувствительны к перезаряду и переразряду, не требуют ухода. Обычные крупные аккумуляторы этим «похвастать» не могут.
На некоторых спутниках связи, космических станциях и даже в бытовых приборах применяются очень дорогие, но зато великолепные по своим характеристикам серебряно-цинковые щелочные аккумуляторы. Им нипочем ни большие токи, ни низкие, до -60 °C, температуры. Они характеризуются плотностью накапливаемой энергии, в пять раз большей, чем кислотные аккумуляторы, а плотностью мощности – вдвое большей.
Всем хорош серебряно-цинковый аккумулятор, хоть сейчас ставь его на автомобиль. Масса аккумулятора для прохождения стокилометрового пути не превысит 100 кг…
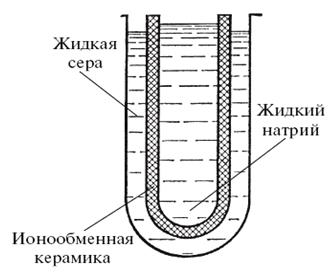
Серно-натриевый аккумулятор
Но, увы, стоимость такого аккумулятора будет во много раз выше стоимости самого автомобиля. И надежд на его удешевление нет никаких – серебра на Земле становится все меньше и меньше, а дорожает оно на мировом рынке все больше и больше. Чтобы аккумулятор мог стать поистине массовым и перспективным, он должен содержать материалы, которых на Земле вдоволь.
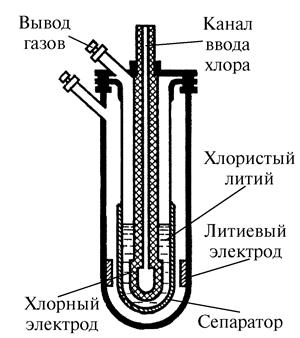
Хлорно-литиевый аккумулятор
Сейчас ученые связывают свои надежды с необычным на первый взгляд аккумулятором, в котором используются гальванические пары «сера – натрий» и «хлор – литий». Металлы там находятся в виде расплавов, их температура достигает нескольких сотен градусов. Расплавленный натрий соединяется в аккумуляторе с горячей жидкой серой, а литий взаимодействует с раскаленным газом – хлором. Из-за того что такие аккумуляторы работают при температурах 300—800 °C, они получили название горячих.
Происходящее внутри горячих аккумуляторов почему-то мне сразу напомнило описание мифологического ада, о котором я в детстве немало читал. Достаточно было представить расплавленную серу, в которой «варится» расплавленный натрий, тот самый натрий, что уже от воды загорается и даже взрывается! О хлоре и говорить нечего – это один из наиболее ядовитых газов, чрезвычайно активный даже при комнатной температуре, а что будет при восьмистах градусах! Недаром ученые уже который год бьются над созданием корпуса к этому «адскому» накопителю – мало какой материал способен выдержать такую начинку.
Однако горячие аккумуляторы при низкой стоимости развивают плотность энергии раз в десять большую, чем свинцово-кислотные аккумуляторы, и плотность мощности у них значительно выше. Если свинцово-кислотные аккумуляторы накапливают в килограмме своей массы 64 кДж энергии, а щелочные – 110, то горячие серно-натриевые – 400—700 кДж!
Автомобилю на 100 км пути хватило бы всего 50 кг серно-натриевого аккумулятора, на 300 км – 150 кг. Это неплохие показатели. Но… горячие аккумуляторы перед началом работы надо разогревать, их оболочка не выдерживает долго «адского» содержимого. Да и при аварии машины с таким аккумулятором оказаться даже в качестве зрителя – тоже небезопасно.
Более спокойный «характер» у новых – медно-литиевых аккумуляторов. Они имеют катод из медного сплава и анод из пористого лития. Электролит органический, с высокой электропроводностью. Плотность энергии у опытных образцов таких аккумуляторов в полтора раза выше, чем у серебряно-цинковых, и, что самое важное, они способны развивать высокую удельную мощность. Если же вместо меди взять фтористое соединение никеля, то и процесс зарядки аккумулятора можно сильно сократить, – всего до нескольких минут.
Интересны аккумуляторы на основе цинка и… обычного воздуха. Цинковый анод здесь просто окисляется кислородом воздуха, поэтому весь запас энергии в аккумуляторе зависит только от количества цинка. Катод изготовлен из пористого никеля и почти не расходуется, а анод по мере износа заменяется новым или восстанавливается пропусканием зарядного тока.
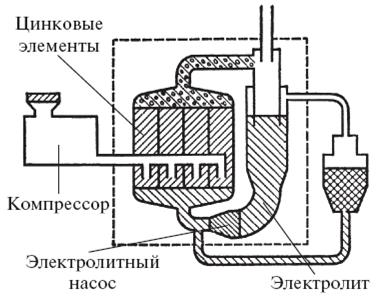
Воздушно-цинковый аккумулятор
Своеобразие этих устройств заключается в том, что они могут работать как в режиме аккумуляторов, так и в режиме обычных гальванических элементов, попросту «сжигая» цинк в кислороде воздуха. Именно в этом случае цинковые аноды приходится заменять, но гальванический элемент при этом будет обладать вдвое большей плотностью энергии по сравнению с аккумулятором.
Однако как ни хороши описанные выше аккумуляторы-рекордсмены, специалисты все-таки считают, что проблему создания современного электромобиля с дальностью пробега 120—150 км должны решить не они, а дешевые и недефицитные никель-цинковые аккумуляторы. По плотности энергии и мощности такие аккумуляторы находятся между обычными и серебряно-цинковыми аккумуляторами.
Тем не менее будущее, хотя и отдаленное, все же за горячими аккумуляторами, несмотря на все трудности и неудобства, связанные с их созданием и эксплуатацией. Их разработкой занимаются самые солидные фирмы и институты, в том числе и у нас в стране. Успехи же весьма скромные – создать конструкцию такого накопителя для серийного производства до сих пор не удалось. Из лабораторий горячий аккумулятор пока не вышел. Вряд ли мне будет под силу тягаться в этом с целыми научными коллективами.
Особенно смутило меня то обстоятельство, что теоретический предел у электрохимических аккумуляторов уже близок. По расчетам ученых, основной показатель аккумулятора – плотность энергии – можно еще повысить максимум в три-четыре раза. Безусловно, маловато получается для «капсулы». Кроме того, как я хорошо знал, подойти вплотную к теоретическому пределу невероятно сложно. Вспомнить хотя бы, сколь трудным оказалось подобраться к абсолютному нулю температуры, к полному вакууму, к совершенно чистым материалам. Подобных примеров можно привести множество из самых разных областей человеческой деятельности.
Поэтому, отдавая должное всесилию электричества и бесспорным преимуществам электроаккумуляторов, я все-таки мечтал найти такой накопитель, теоретический предел которого если не бесконечен, то хотя бы отодвинут достаточно далеко. Лишь тогда можно будет всерьез говорить об «энергетической капсуле».
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
Глава 2. Плюс химизация… всей РККА
Глава 2. Плюс химизация… всей РККА К 1922 г. в наследие от «проклятого царизма» РККА получила около 400 тыс. химических снарядов, в подавляющем большинстве 76-мм. Понятно, что значительная часть их потеряла свое боевое значение.Советское руководство придавало особое значение
ХИМИЯ и СТРЕЛКОВО-АРТИЛЛЕРИЙСКИЕ БОЕПРИПАСЫ
ХИМИЯ и СТРЕЛКОВО-АРТИЛЛЕРИЙСКИЕ БОЕПРИПАСЫ Инженер-полковник И. ГРИШИН, доцент, кандидат технических наукБурный прогресс современной химии привел к тому, что ее достижения оказывают все большее влияние на развитие вооружения, боевой техники и снаряжения. Новые
АВТОМАТИКА ИЛИ ЧЕЛОВЕК ПЛЮС АВТОМАТИКА?
АВТОМАТИКА ИЛИ ЧЕЛОВЕК ПЛЮС АВТОМАТИКА? Вероятно, теперь никто не сомневается в том, что человек должен был проникнуть в космос, окинуть взором нашу Землю с высоты орбитального полета и привезти нам свои непосредственные впечатления. Думается, нет сомневающихся и в том,
Часть 4 ЭЛЕКТРОНИКА И ФИЗИЧЕСКАЯ ХИМИЯ В БТР
Часть 4 ЭЛЕКТРОНИКА И ФИЗИЧЕСКАЯ ХИМИЯ В БТР День, когда мы узнаем, что такое электричество, вероятно, станет ещё более величайшим событием в летописи человечества, чем любое другое происшествие, отражённое в нашей истории. Придёт время, когда комфорт, возможно, даже само
…Плюс информация
…Плюс информация — Столько говорится о планировании, что создается впечатление, будто, кроме него, в АСУ ничего нет. — Есть и другие составляющие формулы АСУ, но все они нацелены на одно — на управление процессом выполнения производственной программы