ГЛАВА 5. Синдром внезапной смерти младенцев
Согласно определению, принятому на II Международной конференции, посвященной проблемам детской смертности, под синдромом внезапной смерти младенцев или синдромом внезапном младенческой смерти (СВМС) понимают неожиданную, ненасильственную смерть ребенка грудного возраста, при которой отсутствуют адекватные для объяснения причин смерти клинические и патолого-анатомические признаки заболевания.
Первые эпидемиологические исследования распространенности СВМС относятся к 60-м годам XX в. Однако только в 80-х были разработаны и приняты в большинстве стран критерии определения синдрома и протокол патолого-анатомического исследования случаев скоропостижной смерти детей раннего возраста. В конце 80-х в большинстве развитых стран от СВМС умирал 1 ребенок из 500 детей первого года жизни. После внедрения национальных программ профилактики СВМС смертность от этого синдрома существенно снизилась: в настоящее время – 1 ребенок на 1300 детей.
Синдром внезапной смерти является одной из основных причин гибели детей в возрасте от 7 дней до года. Распространенность данного синдрома многие исследователи связывают с успехами последних десятилетий в области неонатологии по выхаживанию новорожденных, находящихся в критическом состоянии после рождения. При этом гибель ребенка первого года жизни, имеющего факторы риска, может реализоваться позже при воздействии триггерных факторов в виде синдрома внезапной смерти.
В России на протяжении длительного времени этот синдром как причина смерти не регистрировался. С 1999 г. введена его регистрация в перечне причин смерти как отдельной рубрики. В соответствии с Медицинской классификацией болезней X пересмотра этот синдром обозначается как «внезапная смерть грудного ребенка» в разделе «Неизвестные причины смерти» под рубрикой R 95.
Проблема гибели детей, воспитывающихся в домах ребенка, от СВМС имеет особую актуальность. Анализ смертности воспитанников домов ребенка (Служебное письмо МЗ РФ от 31.05.2000) выявил, что в 22,9 % случаев смерть детей наступила непосредственно в доме ребенка.
Наряду с тяжелой врожденной патологией, ОРВИ и острой пневмонией, синдром внезапной смерти является одной из ведущих причин гибели детей, наступившей непосредственно в стенах интернатного учреждения (около 20 %). Обращает на себя внимание, что в 16,3 % случаев смерть детей наступила в отсутствие персонала. По данным медицинских документов умерших детей, в большинстве домов ребенка не проводилась экспертная оценка летальных случаев.
Случаи неожиданной гибели клинически здорового ребенка первого года жизни известны давно. Долгие годы в повседневной практике бытовал термин «заспать ребенка». Считалось, что мать во сне удушает (неумышленно) спящего с ней в одной кровати ребенка. Предпринимались попытки, чаще всего далекие от медицинского подхода к решению проблемы, уберечь детей. Так, в 1732 г. в Италии была создана специальная камера, в которую помещали спящего ребенка.
Позже случаи СВМС связывали с увеличением тимуса у грудных детей («тимическая смерть»), поскольку при патолого-анатомическом исследовании часто обнаруживалась тимомегалия.
До сегодняшнего дня причины возникновения синдрома внезапной смерти остаются не до конца ясными. Вместе с тем установлены основные закономерности и факторы риска его развития. Известно, что чаще всего СВМС встречается у детей в возрасте 2–4 месяцев, высокий риск сохраняется до 6 месяцев и редко отмечается у детей старше 1 года (в России – 2 % всех случаев). Мальчики страдают в 1,5 раза чаще девочек. Наибольшее количество случаев регистрируется в холодное время года (осень-зима). Описана связь с неблагоприятными метеорологическими условиями. Наиболее опасными являются ночные и ранние утренние часы.
Нередко СВМС развивается вскоре после перенесенной острой респираторной вирусной инфекции, а при аутопсии выявляются минимально выраженные проявления ОРВИ.
Установлены факторы риска развития синдрома внезапной смерти:
I. Социальные факторы
– Вредные привычки родителей (особенно матери).
– Неблагоприятные жилищно-бытовые условия.
– Незарегистрированный брак.
– Низкий образовательный уровень родителей.
– Недостаточный уход и внимание к ребенку.
– Неправильный уход (мягкая подушка, сон на животе, тугое пеленание и др.).
II. Биологические факторы
– Неожиданная смерть другого ребенка в семье.
– Эпизоды очевидных жизнеугрожающих состояний, отмечаемых у ребенка в анамнезе.
– Отягощенный акушерско-гинекологический анамнез матери (аборты, выкидыши, короткие промежутки между родами и др.).
– Юный возраст матери.
– Перинатальные факторы (хроническая внутриутробная гипоксия, недоношенность, задержки внутриутробного развития, внутриутробная инфекция, асфиксия новорожденного, синдром дыхательных расстройств и др.).
– Искусственное вскармливание.
– Недостаточная или избыточная прибавка массы тела, низкий рост, дисгармоничное развитие.
– Атопический или лимфатико-гипопластический тип конституции.
– Дефицит секреторного компонента IgA.
– Вегетативная дисфункция.
Учет факторов риска позволил выделить три основных группы риска по развитию CMC:
– дети, имеющие низкую массу тела при рождении;
– сибсы жертв СВМС (риск развития данного синдрома в 4–7 раз выше, чем в популяции);
– дети, перенесшие очевидные жизнеугрожающие состояния (ОЖС).
Выделение ОЖС в симптомокомплекс связано с фактом возникновения этого состояния у детей, погибших впоследствии от синдрома внезапной смерти. Клинически ОЖС представляет собой эпизод, характеризующийся комбинацией следующих признаков: апноэ, брадикардия, изменение цвета кожи (бледность или цианоз), мышечная гипотония и гипорефлексия, поперхивание. В 80 % случаев ОЖС возникает в период бодрствования детей.
Установлено, что СВМС в значительной мере связан с пост-гипоксическими состояниями, морфо-функциональной незрелостью, задержкой внутриутробного развития. Это предопределяет незрелость регуляторных процессов, приводящую к нарушению основных функциональных систем ребенка. Следствием внутриутробной гипоксии являются нарушения регуляторных центров стволовой части мозга, что вызывает функциональную дезадаптацию ребенка.
Определяющую роль в постановке диагноза СВМС играют результаты патолого-анатомического исследования. По мнению А.В. Цинзерлинга, детей, умерших от синдрома внезапной смерти, можно разделить на две группы:
1) дети с отсутствием каких-либо клинико-анатомических признаков жизнеугрожающих состояний;
2) дети с минимально выраженными клинико-анатомическими признаками ОРВИ.
Результаты внешнего осмотра детей, погибших в результате СВМС, малоспецифичны. Однако среди фенотипических особенностей отмечается распространенность малых аномалий развития: признаки дизморфизма (грыжи, гидроцеле и др.) и диспластические изменения (гемантомы, невусы) встречаются в два раза чаще, чем в популяции. На секции, как правило, обнаруживаются признаки, являющиеся тканевыми маркерами хронической гипоксии:
– избыточное развитие гладкой мускулатуры в артериях легких;
– увеличение массы правого желудочка;
– повышение уровня фетального гемоглобина в крови;
– повышенный внекостномозговой гемопоэз;
– увеличение размеров вилочковой железы;
– гиперплазия хромаффинной ткани, в частности мозгового слоя надпочечников;
– признаки дисфункции надпочечников с аденоматозными разрастаниями и кистами в дефинитивной коре и гигантскими клетками в фетальной зоне коры надпочечников, обилие бурого жира вокруг надпочечников;
– снижение запасов катехоламинов в стволе головного мозга;
– снижение активности допамин-?-гидроксилазы и повышение активности тирозингидроксилазы в гипоталамусе и хвостатом теле;
– достоверное снижение количества миелинових волокон в шейном отделе спинного мозга;
– глиоз ствола головного мозга и демиелинизация периферических нервных волокон;
– отек и набухание головного мозга;
– петехии в серозных оболочках;
– сегментарный отек легких;
– вздутый живот.
Возможные механизмы СВМС до конца не изучены. В научной литературе выдвигаются различные гипотезы. Однако наиболее обоснованы на сегодняшний день две из них:
1) кардинальная (первичная остановка сердца, ведущая к вторичной смерти мозга);
2) респираторная (первичная остановка дыхания с последующей медленной остановкой сердца).
Алгоритм, позволяющий разграничить вероятные механизмы СВМС представлен в табл. 20.
Таблица 20
Патолого-анатомические признаки вероятных механизмов синдрома внезапной смерти (И.М. Воронцов с соавт., 1999)
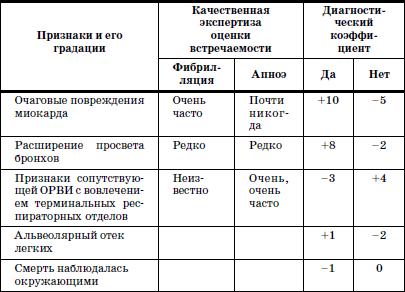
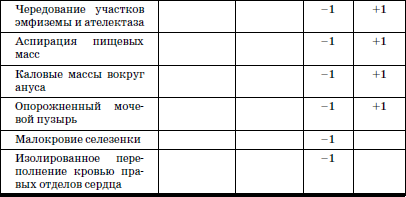
При сумме балов «+13» и более – вероятна смерть в результате фибрилляции желудочков; при сумме «—13» и меньше – вероятная смерть в результате апноэ. Если пороговый уровень не достигнут, ответ неопределенный.
Согласно современным представлениям большое значение в генезе СВМС играет незрелость нервной системы ребенка первых месяцев жизни. Следствием несовершенства регулирующей функции центральной и вегетативной нервной системы может явиться нарушение дыхательной и сердечной деятельности.
Кардиальная гипотеза синдрома внезапной смерти сформировалась в конце 60-х годов. На сегодняшний день она является наиболее обоснованной, так как признаки электрической нестабильности миокарда часто обнаруживаются у детей, перенесших ОЖС и погибших в дальнейшем от СВМС. Кроме того, при патолого-анатомическом исследовании в 27 % случаев обнаруживаются посмертные признаки фибрилляции желудочков (М.А. Школьникова). Реализации кардиальных механизмов способствуют особенности сердечной деятельности детей первого года жизни: при электрокардиографическом исследовании выявляются признаки электрической нестабильности, увеличение QT-интервала, которое достигает максимума в возрасте 2–4 месяцев (пик смертности от СВМС!). Этому способствует нарушение вегетативной регуляции сердца (прежде всего симпатической). Кроме того, известно, что для детей первого года жизни характерно преобладание REM (быстрого) сна в структуре сна. Во время быстрого сна наблюдаются вспышки симпатической и вагальной активности, что приводит к увеличению QT-интервала. Незрелость вегетативной регуляции наиболее характерна для недоношенных, маловесных, функционально незрелых детей.
С этих позиций чрезвычайно важной является правильная организация сна детей, исключающая возможность шума, включение яркого света, появление резких запахов и т. п. в помещении, где спят дети, поскольку эти факторы увеличивают риск возникновения электрической нестабильности миокарда.
Маркерами дисбаланса между симпатическим и парасимпатическим отделами вегетативной нервной системы являются высокая частота сердечных сокращений, снижение вариабельности сердечного ритма и чувствительность барорецепторов. Следует подчеркнуть, что исследование вегетативного статуса воспитанников домов ребенка, проведенное на кафедре поликлинической педиатрии РМАПО, выявило, что сбалансированное состояние вегетативной регуляции имеется лишь у 6 % детей, у 75 % отмечена гиперсимпатикотония.
В достаточной мере обоснованной является также «респираторная» гипотеза. Для детей первого года жизни в период быстрого (REM) сна характерны респираторные паузы и периодическое дыхание. Патологическим является апноэ, продолжительность которого более 20 с, а также более короткая респираторная пауза, если она сопровождается брадикардией, цианозом или бледностью, мышечной гипотонией. Периодическое дыхание не должно превышать 5 % от общей продолжительности сна. При неблагоприятных условиях оно может трансформироваться в апноэ.
Следует отметить, что респираторная пауза, сопровождающаяся нарушением состояния ребенка, является наиболее очевидным предвестником синдрома внезапной смерти (абортивной СВМС) и требует немедленного оказания помощи ребенку. В дальнейшем необходима консультация специалиста и проведение динамического наблюдения за ребенком с применением дыхательного мониторинга.
В научной литературе обсуждаются и другие гипотезы о возможной связи СВМС с различными биохимическими изменениями в организме ребенка. Так, высказывается предположение о связи данного синдрома с нарушением процесса (3-окисления жирных кислот (J.P. Награу). Наиболее явное последствие этого нарушения – приступы гипокетонемии и гипогликемии. Они могут развиваться на фоне кажущегося благополучия при воздействии таких провоцирующих факторов, как голодание ребенка, повышение температуры, инфекционные заболевания и пр. Приступ развивается быстро и может привести к гибели ребенка.
Эту гипотезу подтверждает факт частого обнаружения у детей, погибших от СВМС, признаков жировой дистрофии печени, миокарда, скелетных мышц. Кроме того, в 17 % случаев у детей, имевших эпизоды ОЖС, выявлен дефект (3-окисления жирных кислот.
Существует гипотеза о связи СВМС с нарушениями обмена липопротеидов и витамина Е. Дефицит витамина Е приводит к образованию в организме ребенка избыточного количества перекисных радикалов, нарушению функции печени. Кроме того, повышается сосудистая проницаемость, возникает дыхательная дисфункция, что проявляется обильной транссудацией, пенистыми, сукровичными выделениями из носа. Накопление перекисных радикалов может способствовать гиперплазии мышечного слоя сосудов. Подобные находки нередки при патолого-анатомическом исследовании детей, умерших от СВМС.
Имеется гипотеза о связи СВМС с дефицитом магния (J.K. Miller), нарушением синтеза нейромедиаторов и гормоноподобных пептидов. Было выявлено значительное снижение активности катехоламинсинтезирующих ферментов. Участи детей, погибших от СВМС, выявлена низкая концентрация антагониста эндогенных эндорфинов (субстанции Р). Остановка дыхания у них могла быть вызвана избытком эндогенных наркотических веществ – эндорфинов.
Интересна (с позиций общей профилактики СВМС) гипотеза, связывающая СВМС с «рефлексом паралича страха». «Паралич страха» – это атавистический рефлекс, ответ на чрезмерную внешнюю опасность. Он проявляется продолжительной иммобилизацией, снижением мышечного тонуса, остановкой дыхания на вдохе, брадикардией, периферической вазоконстрикцией.
У детей первых месяцев жизни, воспитывающихся в доме ребенка, развитие подобного рефлекса могут спровоцировать разнообразные ситуации, связанные с несоблюдением персоналом правил ухода и воспитания. Ограничение движений (при тугом пеленании); отсутствие поддержки (подбрасывание ребенка вверх при общении с ним); боль (медицинские манипуляции); резкие незнакомые звуки; внезапное наступление тишины, резкое изменение освещенности и т. п. могут выступить в качестве провоцирующих факторов развития СВМС.
Реакция усиливается, если воздействие фактора происходит во время засыпания. При этом тугое пеленание и ограничение движений ребенка во сне усиливают эффект резких звуков. Показано, что резкое звуковое раздражение во сне вызывают брадикардию, нерегулярное дыхание, трансформирующееся в апноэ.
Профилактика СВМС в доме ребенка
Профилактика СВМС должна охватывать всех детей первого года жизни, поступивших на воспитание в дом ребенка. Профилактическая работа осуществляется в трех направлениях:
1) предупреждение нарушений в уходе за новорожденными и детьми первых месяцев жизни;
2) выявление детей группы риска развития СВМС, проведение превентивной терапии;
3) мониторинг респираторной и сердечной деятельности у детей из группы риска развития СВМС.
С целью выявления детей, относящихся к группе риска развития СВМС, всем новорожденным показано проведение оценки факторов риска (табл. 21).
Таблица 21
Факторы риска развития синдрома внезапной смерти (по М.А. Школьниковой)

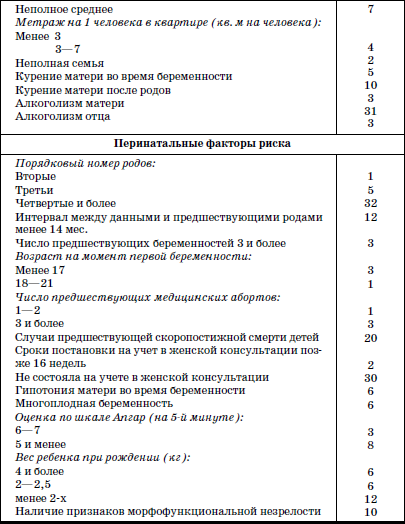
Если оценка риска не была проведена на предшествующих этапах выхаживания ребенка, ее проводят при поступлении малыша в дом ребенка. При выявлении суммы баллов более 70 он относится к группе риска СВМС и требует диспансерного наблюдения[2]:
1) ежемесячные осмотры с обязательной оценкой динамики длины и массы тела;
2) коррекция отклонений в состоянии здоровья (рахит, анемия, гипотрофия и др.);
3) медицинский отвод от профилактических прививок на 6 месяцев;
4) наблюдение невропатолога не реже 1 раза в 6 месяцев;
5) консультация кардиолога и регистрация ЭКГ – 1 раз в 2 месяца, проведение ЭХО КГ в возрасте 1 месяца;
6) консультация в специализированном центре.
При сумме более 100 баллов ребенок относится к группе высокого риска по развитию СВМС. В этом случае показана постановка на учет в специализированном кардиологическом центре. Особое внимание должно уделяться воспитанникам домов ребенка, перенесшим очевидные жизнеугрожающие состояния, недоношенным и имеющим при рождении массу менее 2000 г, детям с признаками морфофункциональной незрелости при нормальных параметрах физического развития.
Эффективным способом профилактики СВМС является строгое соблюдение рекомендаций по уходу за детьми первого года жизни.
– Ребенок должен спать на спине на плотном матрасе, без подушки.
– Нельзя оставлять ребенка одного во время сна – как дневного, так и ночного.
– Необходимо избегать воздействия на ребенка во время сна (в том числе дневного) резких звуков, световых раздражителей, запахов.
– Поддерживать температурный комфорт – не перегревать и не переохлаждать ребенка.
– Избегать тугого пеленания.
– В отсутствие грудного вскармливания молочное питание осуществлять современными адаптированными молочными смесями, обогащенными таурином, карнетином, витаминами, минеральными веществами и т. д.
Учитывая известные закономерности развития СВМС, повышенного внимания требуют дети, болеющие ОРВИ и недавно перенесшие вирусную инфекцию. В течение заболевания и в период реконваленсценции целесообразно обеспечить тщательное наблюдение воспитателей и медицинского персонала за ребенком в период сна. При возникновении жизнеугрожающих состояний необходимо оказать ему неотложную помощь с последующей госпитализаей, обеспечить свободное носовое дыхание и увлажнение воздуха в помещении изолятора или группы, где он пребывает.
Серьезную проблему могут представлять рефлюкс-ассоциированные апноэ, выявляемые у некоторых детей с эпизодами ОЖС (И.М. Воронцов). В этом случае меры, направленные на лечение гастроэзофагеального рефлюкса у детей с исходно высоким риском СВМС, выступают в качестве профилактики развития синдрома.
В последнее время большое внимание уделяется мониторингу респираторной и сердечной деятельности (Информационное письмо МЗ РФ «О методах профилактики синдрома внезапной смерти детей первого года жизни» от 05.03.04). Это исследование позволяет выявлять развитие жизнеугрожающих тахиаритмий и респираторную дисфункцию как потенциальную угрозу СВМС и делает возможным проведение дифференцированной превентивной терапии. В условиях стационара для этих целей используются полифункциональные медицинские мониторы, позволяющие регистрировать кардиореспираторные нарушения.
В условиях дома ребенка целесообразно проведение непрерывного мониторинга дыхательного ритма у детей группы риска в период сна в течение первых 4–6 месяцев жизни.
Кроме того, следует проводить мониторинг дыхания во время сна у детей первого года жизни с признаками ОРВИ и в период реконвалесценции, поскольку этот период опасен с точки зрения развития СВМС. Для мониторинга дыхательной функции в доме ребенка могут быть использованы современные приборы, предназначенные для регистрации респираторной паузы большой продолжительности у новорожденных и детей раннего возраста. Таким образом, в случае тяжелого апноэ, при возникновении необходимости в реанимационных мероприятиях неотложная помощь может быть оказана в кратчайшие сроки.
Медикаментозная превентивная терапия является важнейшей составляющей профилактики СВМС. Она включает:
– нейрометаболическую терапию (глютаминовая кислота, ноотропил, аминалон, глицин и др.);
– применение витаминов-антиоксидантов (витамины А, С, Е) и микроэлементов (селен);
– применение карнитина хлорида (ЭЛЬКАР) и рибофлавина, чередуя их на протяжении всего первого года жизни. Применение кардиореспиторного мониторинга позволяет выявить наиболее вероятные механизмы (кардиальные или респираторные) в случае развития СВМС у конкретного ребенка из группы риска и проводить целенаправленною профилактику.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК