Аккумуляторы
Общими недостатками всех гальванических элементов являются сравнительно малая мощность, отдаваемая во внешнюю цепь, непродолжительное время непрерывной работы, повышенное внутреннее сопротивление, не позволяющее получать ток большой величины. Самый главный их недостаток заключается в том, что в них нельзя восстановить израсходованную электроэнергию. Гальванические элементы можно использовать только один раз.
Более совершенным источником постоянного электрического тока являются аккумуляторы. Слово «аккумулятор» латинское; в переводе на русский язык оно означает «накопитель», «собиратель».
Аккумуляторы по устройству напоминают гальванические элементы. В них имеются положительные и отрицательные электроды, опущенные в электролит. По устройству электродов и составу электролита аккумуляторы делятся на кислотные и щелочные.
Чтобы аккумулятор можно было использовать в качестве источника тока, через него предварительно необходимо пропускать ток от какого-либо постороннего источника постоянного тока. Этот процесс называют зарядкой аккумулятора. Получение тока от аккумулятора называют разрядкой. Аккумуляторы могут давать ток только после зарядки, поэтому их иногда называют вторичными элементами.
Самодельный свинцово-поташный аккумулятор
Существенным недостатком кислотных и щелочных аккумуляторов следует считать неудобство их транспортировки, так как при переноске электролит может выплескиваться из сосудов, попадать на одежду, разрушая ткань. Кроме того, эти аккумуляторы имеют большой вес и габариты. Они выгодны для юных электротехников, когда установлены на одном постоянном месте.
Для различных игр и походов можно изготовить удобные сухие свинцово-поташные аккумуляторы. Они имеют небольшой вес и габариты. Электролит у них сгущен. Их легко переносить и хранить.
Сухой свинцово-поташный аккумулятор показан на рисунке 6.
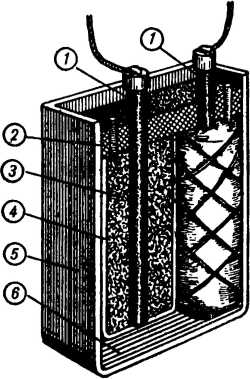
Рис. 6. Простейший свинцово-поташный аккумулятор.
Он состоит из стеклянного или железного сосуда 5, в котором расположены два мешочных электрода. В одном мешочке помещен угольный электрод 1 с активной массой 3 отрицательного полюса, а в другом мешочке — угольный электрод с активной массой положительного полюса. Активная масса в обоих мешочках одинакова по составу — смесь свинцового глета или сурика с порошком графита.
Электролитом служит раствор поташа в воде.
Сухой свинцово-поташный аккумулятор очень легко изготовить.
Подберите какую-либо банку емкостью около пол-литра. Из сухого дерева сделайте круглую или прямоугольную болванку таких размеров, чтобы она заняла примерно половину банки.
Сделайте два одинаковых мешочка 4 из фильтровальной или газетной бумаги. Для этого деревянную болванку неплотно оберните четырьмя-пятью слоями бумаги, не применяя клея. Нижний край бумаги загните на торце болванки подобно тому, как это делается при завертывании бумажки у конфет. Мешочки надо изготовить таких размеров, чтобы они, будучи вставленными в сосуд, плотно прилегали к его стенкам и друг к другу.
Теперь приготовьте активную массу. Для этого возьмите одну весовую часть свинцового глета или сурика в порошке, одну весовую часть графита в порошке и тщательно их перемешайте до получения однородной массы. Чтобы удобнее было обращаться со смесью, увлажните ее слегка электролитом (на 10 весовых частей смеси добавьте 1 весовую часть электролита), причем смесь не должна терять свойства сыпучести.
Подберите два угля от старых гальванических накальных элементов или дуговых фонарей и приступайте к сборке аккумулятора.
Уложите на дно сосуда 20–30 прокладок 6 из газеты. В сосуд вставьте мешочки и заполните их активной массой почти до краев, наблюдая за тем, чтобы не запачкать верхних краев бумажных мешочков. К верхним концам углей прикрепите металлические колечки с отводами. В центры мешочков вставьте угли слегка закругленным концом вниз, при этом угли должны доходить до дна мешочков. При вставке углей не следует сильно нажимать на них, чтобы не прорвать дно мешочка. Массу нельзя подвергать прессовке.
Электролит приготовьте по следующему рецепту. Возьмите 10 весовых частей холодной прокипяченной воды и добавьте в нее 5 весовых частей поташа, все это тщательно перемешайте и наливайте электролит порциями в сосуд до тех пор, пока он не перестанет впитываться. Спустя 1–1,5 часа, когда активная масса поглотит почти все количество залитого электролита, его снова доливают. Чтобы активная масса прочнее связалась с углями аккумулятора, сосуд встряхивают, слегка постукивая его дном по столу. Если в сосуде окажется избыток электролита, его нужно отсосать пипеткой.
Вставьте в активную массу по одной влажной спичке и залейте аккумулятор расплавленной смолой 2 или варом. Когда смола затвердеет, выньте спички. В образовавшиеся отверстия неплотно вставьте деревянные пробочки— и аккумулятор готов. Теперь его надо зарядить.
Средний зарядный ток для сухого аккумулятора 1 ампер на 1 кв. дециметр поверхности любого электрода, а разрядный ток в 5 раз меньше. Емкость достигает до 1,5 ампер-часа на 100 граммов веса аккумулятора. Внутреннее сопротивление — от 0,08 до 0,15 ома на 1 кв. дециметр любого электрода.
Перед тем как приступить к зарядке аккумулятора, надо включить его в зарядную цепь. Один полюс аккумулятора соедините с плюсом источника зарядного тока, а другой полюс — с минусом источника через реостат. Первый электрод аккумулятора обозначьте плюсом (+), а второй — минусом (—). Эта полярность должна строго сохраняться при эксплуатации и последующих зарядках аккумулятора.
Зарядку следует прекратить, как только э. д. с. аккумулятора достигнет 2–2,4 вольта. Перед каждой зарядкой открывают пробочки и заливают по нескольку капель воды. Чтобы получить аккумуляторную батарею, необходимо изготовить несколько таких аккумуляторов и соединить их последовательно.
Самодельный газовый аккумулятор
Известно, что при зарядке обычного кислотного аккумулятора на его аноде выделяется кислород, окисляющий этот электрод, а на катоде выделяется водород. Во время разрядки аккумулятора пластины анода и катода взаимодействуют и происходит обратная реакция, при этом газы водород и кислород играют только вспомогательную роль. Когда аккумулятор отключается от источника зарядного тока, газы бесследно улетучиваются.
В современном газовом аккумуляторе при зарядке газы запасаются в электродах и хранятся в них, как на. «складах», до момента разрядки. Сами электроды не участвуют в химических процессах.
Газовые аккумуляторы относятся к новым источникам постоянного электрического тока. Их достоинством является исключительная простота конструкции, весьма высокая экономичность, так как они не требуют цветных металлов и дорогостоящих материалов. Они очень удобны в эксплуатации: их можно хранить продолжительное время как в заряженном, так и в разряженном состоянии. Эти аккумуляторы не боятся больших зарядных и разрядных токов, что резко сокращает время их зарядки. На такие аккумуляторы не оказывают никакого вредного влияния быстрые разрядки и короткое замыкание.
По конструкции газовый аккумулятор (рис. 7) напоминает свинцово-поташный аккумулятор.
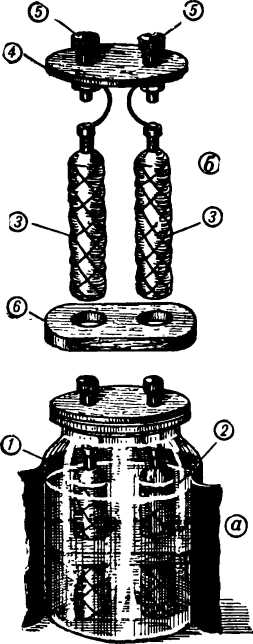
Рис. 7. Простейший газовый аккумулятор и его части (а — общий вид аккумулятора; б — конструкция основных частей): 1 — сосуд; 2 — электролит; 3 — электроды; 4 — крышка; 5 — зажимы; 6 — распорка.
Он состоит из непрозрачного сосуда и двух одинаковых электродов мешочного типа. В каждом мешочке помещается гальванический уголь, окруженный активированным углем.
Электролитом служит раствор поваренной соли.
Принцип работы газового аккумулятора состоит в том, что во время зарядки на его электродах образуются и длительное время сохраняются запасы атомов водорода и хлора. При разрядке аккумулятора эти газы взаимодействуют между собой, создавая электрический ток.
В момент зарядки аккумулятора происходит электролиз раствора. На катоде в мешочке запасается водород, а на аноде — в другом мешочке — запасается хлор. Возникшие во время электролиза атомы водорода и хлора заполняют мельчайшие поры активированного угля и лишаются возможности объединяться в молекулы. Таким образом, применение в электродах активированного угля позволило накапливать запасы газов и содержать их в атомном состоянии.
Газовые аккумуляторы стали возможны после того, как были найдены вещества, обеспечивающие раздельный сбор, хранение и атомный режим газов в аккумуляторе. Такие вещества называют адсорбентами, то есть веществами, обладающими способностью поглощать газы, пары и жидкости.
Явление адсорбции происходит на поверхности поглощающих веществ. Поэтому, чем больше поверхность адсорбентов, тем больше молекул газа или пара они поглощают.
Хорошей поглотительной способностью обладает обычный древесный уголь, так как в нем большая поверхность образуется за счет огромного количества пор.
Самым лучшим адсорбентом является активированный уголь, получаемый в результате специальной обработки обычного древесного угля. В 1 грамме активированного угля общая поверхность достигает 10000 кв. метров. Вот почему в качестве электродов в газовом аккумуляторе был взят активированный уголь.
Простейший газовый аккумулятор легко изготовить самим.
Возьмите стеклянную пол-литровую банку, окрасьте ее снаружи асфальтовым лаком или черной эмалью (можно оклеить черной бумагой). Важно, чтобы свет не проникал внутрь аккумулятора. Любой свет оказывает сильное влияние на газы и разряжает аккумулятор.
Подберите два угольных стержня от накальных элементов или дуговых фонарей. Сшейте два мешочка из хлопчатобумажной ткани. Вставьте в мешочек угольный стержень с прикрепленным выводом на верхнем конце и набейте вокруг него активированный уголь. Зашейте мешочек сверху и плотно обвяжите его прочными машинными или суровыми нитками. Чем больше витков сделаете и сильнее их затянете, тем надежнее будет контакт порошка с угольным стержнем и тем лучше будет работать аккумулятор. Второй мешочек изготовляется таким же способом.
Активированный уголь можно приобрести в магазинах химических реактивов или использовать активированный уголь из старых противогазов. Для получения емкости в 1 ампер-час потребуется 50–90 граммов активированного угля на два мешочка.
Электролит составьте по следующему рецепту. На каждый стакан кипяченой воды всыпьте 1–1,5 столовой ложки поваренной соли. Вставьте мешочки в сосуд и залейте его электролитом. Сосуд закройте деревянной крышкой, пропитанной парафином. Сверху на крышке против электродов укрепите выводы, а в середине крышки сделайте отверстие для заливки и смены электролита. Это отверстие закройте пробкой.
Зарядка газового аккумулятора производится так же, как и обычного кислотного аккумулятора.
Вывод от одного мешочка соедините с отрицательным полюсом источника зарядного тока. Это будет как бы отрицательная пластина аккумулятора (водородный электрод), обозначьте его знаком минус (—). Другой мешочек — с положительным полюсом источника зарядного тока через реостат. Этот мешочек будет служить положительной пластиной (хлористый электрод), обозначьте его знаком плюс (+). Для зарядки одного аккумулятора требуется напряжение 4,5 вольта. Зарядка заканчивается, когда напряжение на зажимах газового аккумулятора будет равно 2,2–2,5 вольта.
Если вы хотите применить эти аккумуляторы в походах, то скрепите их электроды хомутиками из пластмассовых пластинок или из полосок оргстекла, как показано на рисунке 7, а. Распорки не позволят электродам перемещаться.
Для лучшей работы аккумулятора необходимо сменять электролит один-два раза в неделю.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК